La prevenzione primaria e la diagnosi precoce dell’Osteonecrosi delle Ossa Mascellari Farmaco-Relata (Medication-Related Osteonecrosis of the Jaw, MRONJ) sono fondamentali per ridurre l’incidenza e la progressione della malattia. In questo ambito, gli igienisti dentali svolgono un ruolo centrale sebbene, ad oggi, pochissime pubblicazioni hanno proposto protocolli standardizzati e dedicati agli igienisti dentali per la prevenzione della MRONJ. Lo scopo di questo articolo è quello di fornire una raccomandazione aggiornata, con riferimento al ruolo dell’igienista dentale, per la prevenzione della MRONJ.
Il presente lavoro rappresenta l’aggiornamento delle buone pratiche definite e condivise durante la ONJ Consensus Conference del 2021 (ONJ update, 9 Maggio 2021, www.onjupdate.it), in cui hanno partecipato 11 esperti italiani (i.e. igienisti dentali rappresentanti le principali società scientifiche – AIDI e UNID – e oncologi, chirurghi maxillo-facciali e dentisti, promotori delle raccomandazioni del 2020) e pubblicate nel 2022 in lingua inglese sulla rivista internazionale Supportive Care in Cancer.
Il protocollo descritto è incentrato sul ruolo dell'igienista dentale nella gestione dei pazienti a rischio o con MRONJ conclamata e riguarda tre principali step: prevenzione primaria, prevenzione secondaria e supporto al trattamento della MRONJ. Per ogni step sono riportate indicazioni e procedure per l'igienista dentale.
INTRODUZIONE
L’osteonecrosi delle ossa mascellari farmaco-relata (Medication-Related Osteonecrosis of the Jaw, MRONJ) è definita una “reazione avversa farmaco-relata, caratterizzata dalla progressiva distruzione e necrosi dell’osso mandibolare e/o mascellare di soggetti esposti al trattamento con farmaci per cui sia accertato un aumentato rischio di malattia, in assenza di un pregresso trattamento radiante” (1–3).
I farmaci associati al rischio di MRONJ sono i “Bone Modifying Agents” (BMA) (i.e, bisfosfonati o denosumab) e/o i farmaci anti-angiogenici (AA) (e.g., bevacizumab, etc.) (4–10).
Negli ultimi anni, le categorie di pazienti a rischio di MRONJ sono gradualmente cambiate a causa dell’introduzione di nuovi farmaci sul mercato e dell’approvazione di nuove indicazioni per farmaci già in uso. I pazienti a rischio di sviluppare MRONJ sono adesso classificati in due grandi macrocategorie in base all’ assunzione di 1) BMA ad alto dosaggio e/o di AA, versus, 2) BMA a basso dosaggio. I pazienti che generalmente assumono BMA sono: (3, 10–12):
- pazienti oncologici con metastasi ossee (Bone Metastasis, BM) o con mieloma multiplo, trattati con alte dosi di BMA (HD-BMA);
- pazienti affetti da Tumore gigantocellulare dell’osso (TGC) trattati con un’iniezione mensile di Denosumab (HD-BMA);
- pazienti affetti da carcinoma mammario o prostatico, solitamente senza BM e sottoposti a terapia ormonale, trattati con basse dosi di BMA (LD-BMA), allo stesso dosaggio dei pazienti osteometabolici, per prevenire la perdita di densità ossea secondaria alle terapie oncologiche (Cancer Treatment Induced Bone Loss, CTIBL) (10);
-
pazienti osteometabolici in terapia con LD-BMA.
L’Osteonecrosi delle Ossa Mascellari Farmaco-relata è una patologia che può influenzare in larga misura la qualità di vita dei pazienti che ne sono affetti (3, 10). Sebbene la sua eziopatogenesi sia ancora incerta, l’incidenza, la gravità e la progressione della MRONJ può essere fortemente ridotta grazie alle strategie di prevenzione primaria e secondaria (13–15).
La gestione dei pazienti a rischio di sviluppare MRONJ, o già affetti dalla malattia, è multidisciplinare dal momento che sono coinvolti diversi professionisti della salute (e.g., oncologo, bone specialist, odontoiatra, chirurgo orale o maxillo-facciale, igienista dentale). Nonostante, sul piano teorico, il ruolo dell’igienista dentale risulti fondamentale per le misure di prevenzione della MRONJ, ad oggi, solo due studi hanno investigato la suddetta tematica. Uno di essi, ha analizzato il grado di awareness degli igienisti dentali sulla MRONJ, e, il secondo il ruolo degli igienisti dentali nella prevenzione della MRONJ focalizzandosi sui casi associati alla presenza di protesi mobili incongrue (16–18).
Anche la Società Italiana di Ortopedia e Traumatologia (SIOT) e la Società Italiana di Parodontologia e Implantologia (SIdP) hanno dato il loro contributo attraverso la pubblicazione di un Joint Report nel quale sono state proposte delle raccomandazioni di buona pratica clinica che mirano al raggiungimento di un approccio integrato (e.g., prescrittore, odontoiatra, parodontologo e igienista dentale) nella gestione dei pazienti con parodontite sottoposti a terapia con LD-BMA per disturbi osteometabolici per ridurre il rischio di MRONJ (19).
Nel 2021 si è tenuta una Consensus Conference, cui hanno partecipato 11 esperti italiani (i.e. igienisti dentali afferenti alle principali associazioni tecnico scientifiche – Associazione Nazionale di Rappresentanza degli Igienisti Dentali (AIDI) e Unione Nazionale Igienisti Dentali (UNID) – e gli autori delle Raccomandazioni della Società Italiana di Patologia e Medicina Orale (SIPMO) e della Società Italiana di Chirurgia Maxillo-Facciale (SICMF). Il presente board multidisciplinare, tenendo in considerazione le buone pratiche descritte nelle Raccomandazioni italiane SIPMO-SICMF sulla MRONJ (2020) e nella Consensus Conference Italiana (20), aveva discusso specifiche problematiche riguardanti la MRONJ. I risultati condivisi, riguardanti la professione dell’igienista dentale, sono stati pubblicati nel 2022 in lingua inglese sulla rivista internazionale Supportive Care in Cancer (21). Il presente articolo è redatto in lingua italiana, aggiornato, revisionato e approvato all’unanimità dal board.
Per facilitarne la comprensione, conditio sine qua non è la conoscenza delle categorie di pazienti a rischio di MRONJ, dei fattori di rischio (e.g., farmaco-relati, sistemici e locali), dei criteri diagnostici clinico-radiologici e della stadiazione della patologia. Le nozioni relative a questi argomenti sono state descritte nelle Raccomandazioni clinico-terapeutiche sull’osteonecrosi delle ossa mascellari (ONJ) farmaco-relata e sua prevenzione del 2020, consultabile gratuitamente online (23).
È ormai ampiamente dimostrata l’importanza della prevenzione e della gestione multidisciplinare di questa patologia; pertanto, questo studio si propone di raccogliere e analizzare le best practices cliniche presenti in letteratura, con particolare attenzione al Position Paper italiano del 2024, aggiornamento in lingua inglese delle precedenti Raccomandazioni italiane, e al Joint Report della SIOT-SIdP (19, 21). Il primo studio analizza tutte le categorie di pazienti a rischio di MRONJ, fornendo indicazioni sulla prevenzione primaria, secondaria e terziaria (21). Il secondo, invece, si concentra esclusivamente sui pazienti in terapia con LD-BMA per patologie osteometaboliche, soffermandosi principalmente sulla prevenzione primaria (19).
Prevenzione primaria
Un corretto approccio preventivo rappresenta la strategia più efficace al fine di tutelare la salute orale del paziente che dovrà assumere, assume o ha assunto BMA e/o AA (22–24).
Nello specifico, l’obiettivo della prevenzione primaria è il controllo (limitazione/eliminazione) dei fattori di rischio locali della MRONJ sia prima sia durante l’assunzione dei farmaci ONJ-relati.
La finalità della prevenzione primaria, eseguita periodicamente (e non solo prima dell’assunzione del farmaco) è quella di mantenere e/o ripristinare un buono stato di salute dento-parodontale del paziente per il raggiungimento di due obiettivi (3, 21):
- procedure conservative (non invasive), che verranno eseguite dall’odontoiatra e dall’igienista dentale, per ridurre la possibilità di insorgenza o progressione di eventi infettivi/infiammatori (fattori di rischio locali di MRONJ);
- procedure invasive (e.g., avulsioni dentarie), che verranno eseguite dall’odontoiatra, in presenza di elementi dentari con prognosi dubbia o infausta (non trattabili mediante procedure conservative).
Un’ulteriore finalità della prevenzione primaria è l’attività di counselling, che è compito dell’odontoiatra e dell’igienista dentale, mediante la quale il paziente viene informato del rischio di sviluppare MRONJ e reso edotto delle sue eventuali manifestazioni cliniche, in modo da poter allertare tempestivamente e favorire la diagnosi precoce e la terapia della malattia.
Tutte le condizioni che direttamente o indirettamente compromettono uno status di salute orale ottimale, soprattutto a livello dento-parodontale, rendendo le ossa mascellari maggiormente suscettibili alle infezioni, compreso le sollecitazioni meccaniche croniche, sono da considerare importanti fattori di rischio per l’insorgenza di MRONJ, soprattutto nei pazienti in terapia con HD-BMA o LD-BMA da più di tre anni (2, 6, 25, 26).
Pertanto, l’igienista dentale ha un ruolo centrale nella prevenzione della MRONJ in quanto durante i richiami periodici, oltre che dell’igiene orale professionale, si occuperà anche di:
- controllare i fattori di rischio locali;
- mantenere e/o ripristinare lo stato di salute orale dento-parodontale;
- mantenere/migliorare l’adherence e concordance del paziente alle manovre di igiene orale domiciliare.
Nei pazienti sottoposti a terapia con HD-BMA, le procedure di prevenzione primaria dovrebbero iniziare sempre prima dell’inizio della terapia, come da Raccomandazioni Ministeriali (27, 28), e proseguire durante e dopo il trattamento (28). Diversamente, nel paziente sottoposto a terapia con LD-BMA, dato il basso rischio di sviluppare MRONJ, si consiglia di iniziare le procedure di prevenzione primaria entro e non oltre i 6 mesi dall’inizio della terapia con farmaci ONJ-relati (Tabella 1) (2). Secondo il Joint Position Paper della SIOT e SIdP, i pazienti osteoporotici in procinto di iniziare terapia con LD-BMA devono quindi essere indirizzati per un esame odontoiatrico e parodontale completo prima di iniziare il trattamento e la terapia parodontale deve essere eseguita prima di iniziare la terapia con LD-BMA (19). Durante la visita pre-terapia, l’odontoiatria rilascerà un report al paziente sul suo stato di salute orale e la prognosi degli elementi dentari affetti da patologie (e.g., carie, parodontite), e indicherà le eventuali cure necessarie a cui il paziente dovrà sottoporsi in tempi brevi con relativo parere favorevole o sfavorevole per iniziare la terapia con BMA (Figura 1a e 1b).

Fasi operative di prevenzione primaria in pazienti in attesa di iniziare la terapia con farmaci ONJ-relati (prevenzione primaria pre-terapia)
Durante la prima visita saranno definite le misure di prevenzione primaria di MRONJ sulla base della valutazione dello stato di salute orale del paziente (e.g., salute parodontale, gengivite, parodontite) (Tabella 2). L’acquisizione della documentazione clinica e radiologica in possesso del paziente ci darà le prime indicazioni sulle condizioni di salute dello stesso (29).
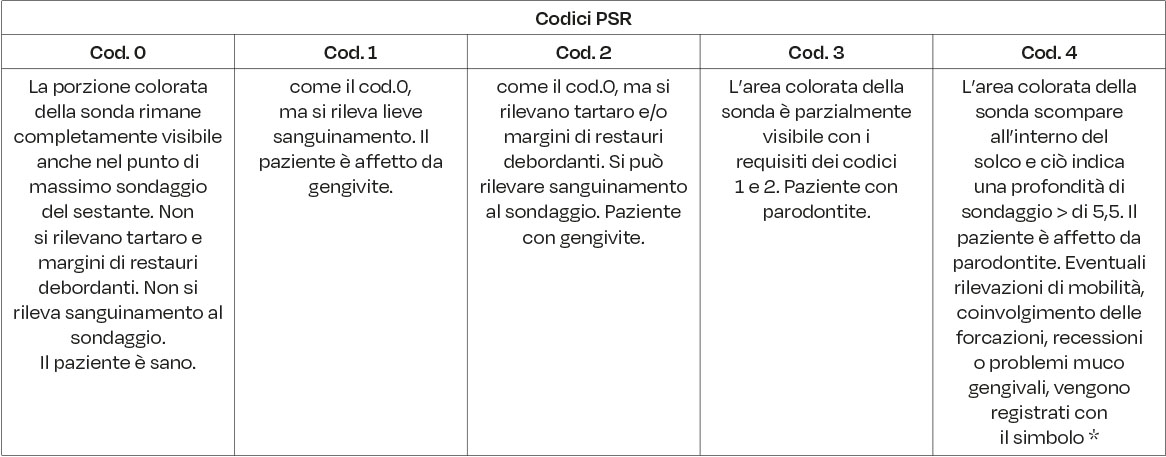
Pertanto, le valutazioni cliniche iniziano con le procedure di screening dello stato di salute dei tessuti parodontali e degli elementi dentali. Il board suggerisce l’utilizzo del Periodontal Screening and Recording (PSR) (30). Tale metodica è indicata per differenziare rapidamente i quadri clinici e individuare eventuali segni di parodontite (e.g. charting parodontale). Il PSR è una procedura efficace e applicabile a ogni paziente (31). A tal fine ricordiamo la possibilità di utilizzare la sonda parodontale WHO o la sonda North Carolina (Tabella 3). Inoltre, durante lo screening l’igienista dentale potrà anche valutare la presenza di eventuali lesioni cariose, che saranno prontamente segnalate all’odontoiatra.
Anche la SIOT e la SIdP consigliano l’acquisizione di un’ortopantomografia recente per una valutazione completa e la successiva registrazione della profondità di sondaggio parodontale (PD), dell’indice di sanguinamento al sondaggio (BOP) e della perdita ossea radiografica (RBL) per completare la diagnosi parodontale. Deve inoltre essere valutato l’indice di igiene orale, ovvero il livello di controllo domiciliare del biofilm da parte del paziente. Successivamente, è necessario definire staging e grading per stabilire la terapia parodontale adeguata e raggiungere il controllo dell’infiammazione (19). È ampiamente condiviso che, in presenza di elementi dentari con prognosi infausta, sia preferibile eseguire, ove possibile, le procedure chirurgiche necessarie prima di avviare la terapia con BMA (19, 21). Dopo le valutazioni dello stato di salute orale, è consigliata la rivalutazione di tutti i fattori di rischio locali (potenziali o presenti). In presenza di protesi amovibile, dovrà essere valutata la congruità, la stabilità e il livello di manutenzione della stessa (e.g., assenza di asperità, integrità del manufatto protesico) (2, 32). In presenza di protesi fisse deve essere valutato il sigillo marginale (e.g., margini debordanti, presenza di carie secondarie), i rapporti tra gli elementi intermedi (se presenti) e i tessuti molli, oltre alla capacità del paziente di eseguire le corrette manovre di igiene orale domiciliare.
È inoltre consigliabile eseguire la valutazione delle mucose orali al fine di identificare eventuali lesioni/neoformazioni, che andranno riportate in cartella e registrate mediante report fotografico. In presenza di eventuali lesioni alle mucose e/o infezioni opportunistiche, l’igienista dentale invierà il paziente all’odontoiatria esperto in medicina orale, o specialista in chirurgia orale, o nei centri di riferimento per la diagnosi e cura di MRONJ (21). Gran parte del successo terapeutico delle misure di prevenzione, risiede nelle capacità dell’igienista dentale di coinvolgere il paziente al punto da indurre dei cambiamenti comportamentali per il controllo dei fattori di rischio locali e sistemici modificabili (33, 34). Il paziente, solo se adeguatamente motivato e istruito, sarà in grado di eseguire pratiche di igiene orale domiciliare efficaci (2). Risulta, quindi, di fondamentale importanza una buona capacità di osservazione, ascolto e comunicazione (30). Le indicazioni sulle tecniche di igiene orale domiciliare saranno definite in base allo stato clinico generale, alla morfologia del cavo orale e degli elementi dentari, al fenotipo gengivale, alla collaborazione del paziente e alle attitudini manuali dello stesso. La scelta e l’utilizzo dei presidi di igiene orale domiciliare deve essere concordata con il paziente, tenendo conto dei tempi di apprendimento e concordando la necessità di applicazione, le modalità e gli strumenti da utilizzare (30). Si raccomanda lo spazzolamento manuale o elettrico degli elementi dentali come mezzo principale per il controllo della placca, prediligendo filamenti soft. In presenza di infiammazione gengivale, la detersione interprossimale, preferibilmente mediante l’utilizzo di scovolini interdentali, deve essere impartita direttamente sul paziente. Il clinico potrà suggerire altri dispositivi/metodi di detersione interdentale (e.g., fili, spazzolino monociuffo) in modo personalizzato e adeguato al caso (35).
La scelta del dentifricio dovrebbe agevolare un giusto apporto di minerali; è consigliato un dentifricio specifico scelto in base alle necessità del caso (e.g., fluorato, desensibilizzante, con enzimi, con probiotici) (30).
Il controllo chimico, come adiuvante del controllo meccanico della placca, sarà affidato all’utilizzo di collutori/gel antibatterici, in base alle varie fasi del percorso terapeutico o di mantenimento. In letteratura l’efficacia di diverse sostanze è stato ampiamente oggetto di studio e sembrerebbe che i collutori antisettici a base di clorexidina abbiano un buon effetto sul microbioma orale (36, 37).
In presenza di protesi inamovibili è necessario istruire il paziente all’utilizzo del filo interdentale dotato di ago passafilo o estremità semi-rigida che permetta l’inserimento tra gli elementi protesici e/o eventuale utilizzo dell’idropulsore, poiché al di sotto delle protesi possono accumularsi facilmente residui alimentari e placca difficilmente asportabili con il solo spazzolamento (21).
In presenza di impianti, gli strumenti per l’igiene domiciliare non devono presentare parti metalliche che potrebbero provocare rugosità e favorire l’accumulo di placca e tartaro. In presenza di protesi amovibili andrà consigliata la loro detersione giornaliera mediante l’uso di spazzolini e prodotti dedicati. Nel caso di protesi amovibili su impianti (i.e., overdenture) bisognerà istruire il paziente alla detersione di tutte le componenti (e.g., fixture, abutment, attachments), oltre che della protesi (21). L’igienista dentale deve rendere il paziente partecipe e consapevole dell’importanza dell’autovalutazione nell’intercettare eventuali segni o sintomi precoci di MRONJ (e.g., mobilità improvvisa degli elementi dentari, ascessi, dolore, alitosi), affinché possa essere egli stesso promotore della diagnosi precoce (2, 12).
In presenza di abitudini voluttuarie (e.g., tabagismo) sarà cura dell’igienista dentale l’attivazione delle tecniche di counselling dedicate (21). La fase successiva è l’esecuzione delle procedure d’igiene orale professionale. L’ablazione tartaro comprende interventi volti all’eliminazione della placca e del tartaro, nonché l’identificazione di eventuali fattori di ritenzione (e.g., otturazioni debordanti) che potrebbero compromettere le pratiche di igiene orale (21).
Durante il trattamento professionale la scelta degli strumenti e delle tecniche, dovrebbero privilegiare sempre azioni poco invasive nel rispetto dei tessuti orali tenendo sempre conto delle condizioni cliniche. È fondamentale l’uso di estremità lavoranti adeguate al sito da trattare sia con strumentazione manuale, sia meccanica (e.g., sonica/ultrasonica). Ad oggi, nella terapia parodontale non chirurgica, il debridement ad ultrasuoni risulta efficace per la rimozione del tartaro (35). Per la rimozione del biofilm (deplaquing), risultano di supporto gli strumenti con tecnologia di ultima generazione (e.g., air polishing) attraverso l’utilizzo di polveri a ridotta granulometria (38, 39). Il loro impiego è indicato anche in presenza di riabilitazioni implanto-protesiche. È possibile utilizzare un rivelatore di placca (preferibilmente a colorazione bi o trifasico), prima di procedere al deplaquing, per facilitarne l’identificazione e la rimozione. In presenza di malattia parodontale la seduta d’igiene orale professionale dovrà comprendere il debridement sottogengivale privilegiando strumenti minimamente invasivi (e.g., inserti sottili e/o curette mini o micro-mini five), se necessario, in anestesia locale (38, 39).In presenza di comorbidità, sarà compito dell’odontoiatra valutare la necessità di un eventuale profilassi antibiotica (e.g., rischio di endocardite batterica) (40).
Sulla base delle condizioni di salute generale del paziente, sarà cura dell’operatore valutare la modalità di trattamento (approccio a quadranti o modalità full-mouth) (38, 39).
Il paziente in pre-terapia affetto da parodontite sottoposto a trattamento di igiene professionale deve essere rivalutato entro 30 giorni dalla fine del trattamento (2).
Il quadro clinico atteso è la guarigione dei tessuti parodontali, che permetterà di inserire il paziente in follow-up a 4 mesi se in terapia con HD-BMA e a 6 mesi se in terapia con LD-BMA (Figura 2) (2). Sulla base degli indici rilevati dal PSR, si possono programmare incontri periodici personalizzati (2). Poiché è ormai ampiamente dimostrato che la prevenzione e il controllo dell’infiammazione orale riducono il rischio di MRONJ, sia il Position Paper per Igienisti Dentali sia il Joint Position Paper SIOT-SIdP adottano un approccio basato sul rischio individuale del paziente per la gestione del follow-up (19, 21). Tuttavia, il Position Paper per Igienisti Dentali fornisce un protocollo con intervalli più o meno precisi per le visite di controllo (4-6 mesi a seconda delle dosi di BMA e della presenza di eventuali fattori di rischio) (21), mentre il Joint Position Paper SIOT-SIdP lascia maggiore flessibilità nella definizione della frequenza delle visite (19). Per chiarezza, si esemplificano qui di seguito le condizioni parodontali, sulla base del codice PSR (Tabella 4), in cui si può trovare il paziente candidato alla terapia con BMA e/o AA.
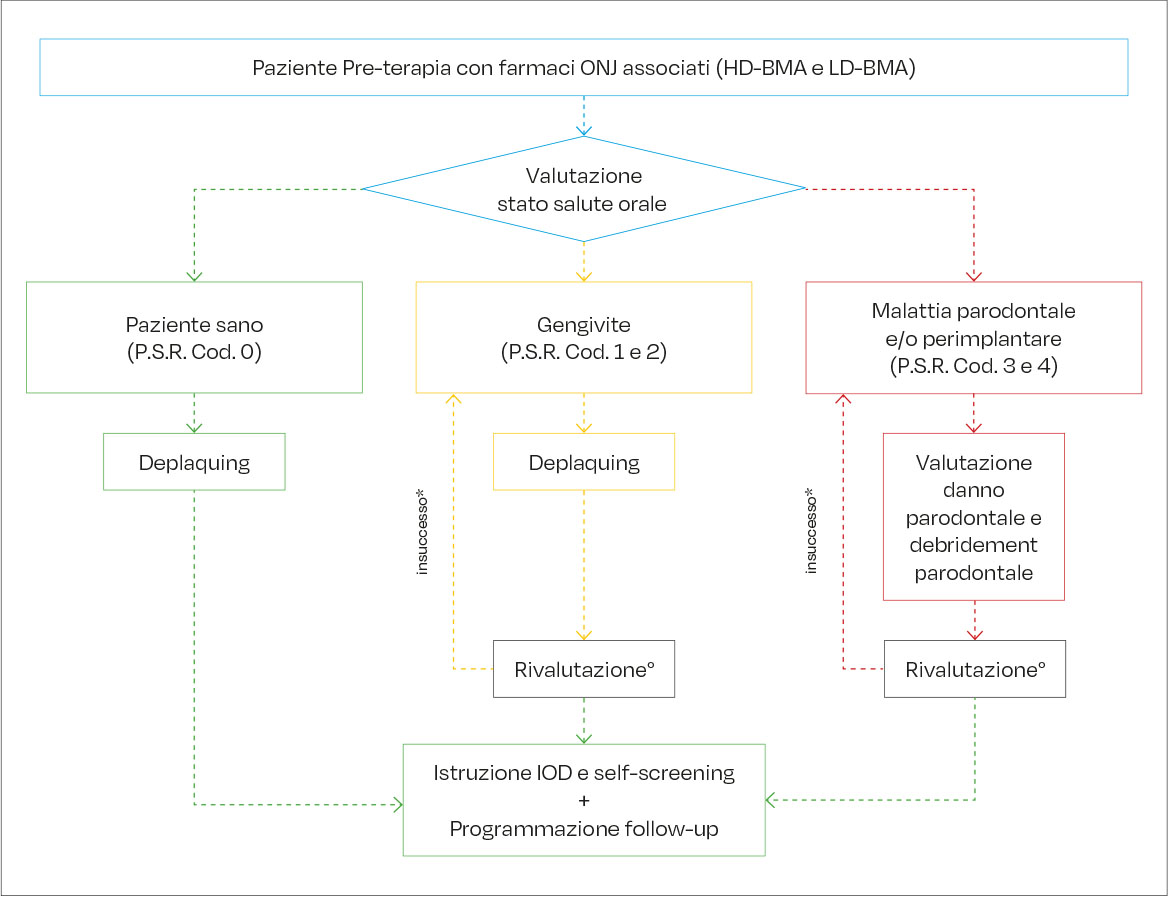
Paziente sano (PSR Cod. 0)
In assenza di segni clinici di infiammazione, il paziente deve essere considerato, dal punto di vista parodontale, sano (Cod. 0) (41–43). Il paziente va comunque motivato sull’importanza del mantenimento della salute orale e dell’autovalutazione per l’intercettazione di eventuali segni o sintomi precoci di MRONJ. I pazienti in terapia con HD-BMA verranno sottoposti a controlli odontoiatrici periodici ogni 4 mesi, mentre i pazienti in terapia con LD-BMA verranno sottoposti a controlli odontoiatrici periodici ogni 6 mesi (Figura 2).
In presenza di gengivite e/o mucosite (PSR Cod. 1 e 2)
I codici 1 e 2 del PSR indicano una salute orale inadeguata. Dopo avere eseguito le misure descritte in tabella 2, il paziente verrà rivalutato orientativamente entro i 30 giorni successivi (41–43). La rivalutazione permetterà di verificare la risposta tissutale al trattamento, l’efficacia delle tecniche di controllo della placca attuate dal paziente e, laddove necessario, offrirà la possibilità di correggere manovre inadeguate. In presenza di riabilitazioni implanto-protesiche, andrà valutata l’eventuale presenza di segni e sintomi compatibili con la presenza di mucosite (e.g., Bleeding on Probing, BoP). Il paziente sarà trattato con gli strumenti appropriati per le manovre di igiene orale su impianti (e.g., punte in teflon) (44). Se le misure attuate risulteranno efficaci, il paziente sarà inserito in follow-up a medio-lungo termine (HD-BMA ogni 4 mesi, LD-BMA ogni 6 mesi) (2). Di contro, se alla rivalutazione persisterà un quadro clinico d’infiammazione, l’igienista dentale individuerà le cause dell’insuccesso correggendole e ripeterà le misure di prevenzione, fino ad ottenere un adeguata adesione alle strategie di prevenzione (Figura 2).
In presenza di malattia parodontale e/o perimplantare (PSR Cod. 3 e 4)
Nel paziente che alla valutazione iniziale presenta chiari sintomi di malattia parodontale identificati attraverso i codici 3 e 4, l’igienista dentale procederà con una valutazione approfondita dello status parodontale (charting parodontale) (41–43). In questo sottogruppo di pazienti, il trattamento può essere realizzato attraverso tecniche di debridement parodontale convenzionali. In presenza di mobilità dentaria, la continua sollecitazione dei tessuti, può determinare disagio e indurre il paziente ad evitare il fisiologico utilizzo degli elementi compromessi, e ancor più a ridurre le manovre di detersione degli stessi. Valutato il grado di mobilità e la prognosi degli elementi dentari, si può considerare lo splintaggio degli elementi mobili. Allo stesso modo, in presenza di segni e sintomi di perimplantite, andranno eseguite le manovre di igiene orali previste per il trattamento di questa patologia (45). La rivalutazione dopo il trattamento parodontale non chirurgico dovrà essere eseguita entro 30 giorni dalla fine del trattamento (2). Il quadro clinico atteso è la guarigione dei tessuti parodontali, che permetterà di inserire il paziente in follow-up a 4 mesi se in terapia con HD-BMA e a 6 mesi se in terapia con LD-BMA (Figura 2) (2). In caso di persistenza di focolai infiammatori (sondaggi superiori o uguali a 4 mm con BoP positivo), si deve considerare la possibilità di eseguire nuovamente le misure terapeutiche non chirurgiche, rinforzando le istruzioni e motivazione, o valutare con l’odontoiatra strategie di prevenzione alternative, compatibilmente con la patologia primaria del paziente (21). Nei pazienti candidati a iniziare la terapia con HD-BMA, si consiglia comunque di attivare il percorso terapeutico nel più breve tempo possibile, per agevolare l’inizio della terapia oncologica (2). Per i pazienti candidati a iniziare la terapia con LD-BMA, i trattamenti potranno essere eseguiti entro i primi sei mesi dall’inizio della terapia (2).
Il Board ritiene che per i pazienti candidati a iniziare la terapia con HD-BMA, la valutazione dello stato di salute dento-parodontale, si debba eseguire SEMPRE PRIMA dell’inizio dell’assunzione di farmaci ONJ-relati, mediante la valutazione clinica e l’imaging radiologico. Le eventuali patologie dei tessuti parodontali andranno trattate tempestivamente, al fine di ridurre il rischio di MRONJ.
Nei pazienti in attesa di iniziare la terapia con LD-BMA, la valutazione odontoiatrica iniziale non è perentoria prima dell’inizio dell’assunzione degli stessi, ma si consiglia venga effettuata ENTRO e non oltre I PRIMI 6 MESI di terapia. Inoltre, si reitera la necessità del rinforzo motivazionale e delle indicazioni ai pazienti utili per l’auto-valutazione.
Fasi operative di prevenzione primaria durante la terapia con farmaci ONJ-relati (prevenzione primaria in- o post-terapia)
Nel caso in cui il paziente si presenta a visita odontoiatrica in corso di terapia con farmaci ONJ-relati (o dopo il termine della stessa), come di consueto l’odontoiatra eseguirà la raccolta dei dati anamnestici e l’esame clinico-radiologico, valuterà il rischio di MRONJ e la presenza o meno di fattori di rischio locali (2). Come per i pazienti in pre-terapia con farmaci ONJ-relati, anche in questo caso andrà ripetuta la sequenza di azioni svolte dall’igienista dentale descritte in Tabella 2. Inoltre, è fondamentale ricordare che nei pazienti che hanno assunto farmaci ONJ-relati sarà importante applicare anche le misure di prevenzione secondaria oltre quelle di prevenzione primaria (2). Sulla base degli indici rilevati del PSR, si eseguiranno misure di prevenzione mirate e si programmeranno visite di follow-up periodiche personalizzate. Ad ogni controllo successivo bisognerà aggiornare sempre l’anamnesi medica, e in particolare le notizie relative all’assunzione dei farmaci ONJ-relati (21).
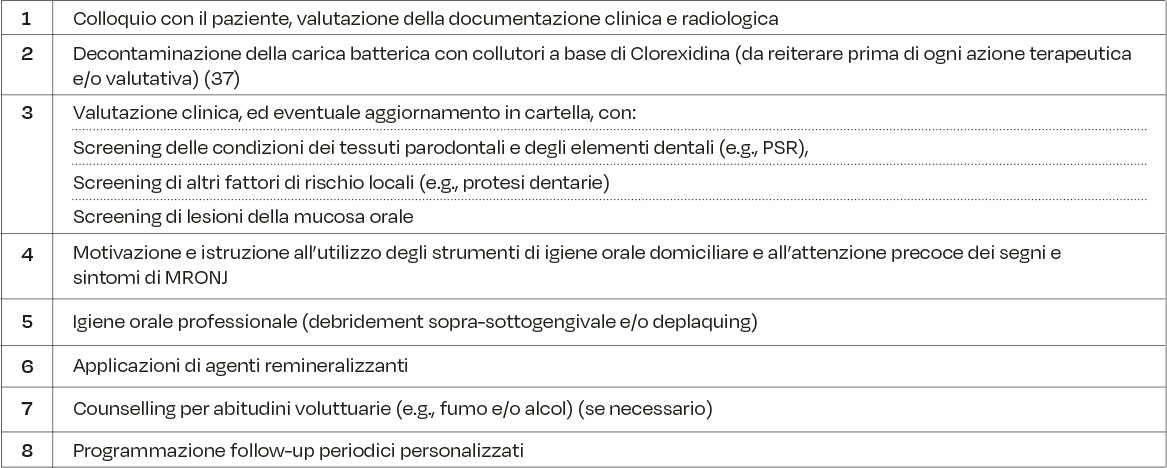
Per chiarezza, si esemplificano qui di seguito le condizioni parodontali, sulla base del Codice PSR, in cui si può trovare il paziente in terapia con farmaci ONJ-relati.
Paziente sano (PSR Cod. 0)
In assenza di segni di infiammazione gengivale, il paziente andrà inserito in follow-up periodico ogni 4 mesi se in terapia con HD-BMA e ogni 6 se in terapia con LD-BMA (Figura 3) (2).
Paziente con gengivite (PSR Cod. 1 e 2)
In presenza di gengivite (Cod. 1 e 2), bisogna agire tempestivamente per la risoluzione dell’infiammazione per evitare che essa possa evolvere in malattia parodontale (2). Pertanto, in presenza di placca e tartaro, si procederà alla rimozione attraverso l’utilizzo di strumenti meccanici e/o manuali con tecniche meno invasive possibili. Il paziente sarà rivalutato entro 30 giorni; se le misure attuate risulteranno efficaci, il paziente sarà inserito in follow-up a medio-lungo termine (HD-BMA ogni 4 mesi, LD-BMA ogni 6 mesi) (21). Nel caso persista la gengivite bisognerà sottoporre il paziente a nuove sedute di igiene orale e d’istruzione e motivazione all’utilizzo degli strumenti di igiene orale domiciliare (Figura 3).
Paziente con malattia parodontale (PSR cod. 3 e 4)
Nei pazienti in corso di terapia con farmaci ONJ-relati, in cui vengono rilevati codici 3 o 4 del PSR, l’igienista dentale approfondirà la valutazione iniziale andando a indagare il danno tissutale attraverso il sondaggio parodontale (e.g., clinical attachment level o CAL, PPD, BoP), al fine di avere una reale misura della perdita dei tessuti parodontali (21).
Relativamente ai protocolli, si faccia riferimento a quanto precedentemente descritto per i pazienti in prevenzione pre-terapia con farmaci ONJ-relati. In presenza di comorbidità, sarà compito dell’odontoiatra verificare la necessità di sottoporre il paziente a copertura antibiotica (e.g., rischio di endocardite batterica). La rivalutazione dello stato di salute, dopo il trattamento parodontale non chirurgico, dovrà essere eseguita entro 30 giorni dalla fine del trattamento. Il quadro clinico atteso è la guarigione dei tessuti parodontali, che permetterà di inserire il paziente in un percorso di follow-up standardizzato (4 mesi se in terapia con HD-BMA, 6 mesi se in terapia con LD-BMA) (Figura 3) (2). La persistenza di focolai infiammatori richiederà il ritrattamento, rinforzando nuovamente le istruzioni e motivazioni all’igiene orale domiciliare. Ricordando che questo processo educativo deve assumere carattere dinamico, capace quindi di adattarsi alle diverse caratteristiche del paziente o qualora necessario, di rimodularsi davanti a difficoltà di apprendimento. Al tempo stesso, bisognerà valutare con l’odontoiatra strategie di prevenzione primaria alternative (e.g., avulsione dentaria), compatibilmente con la patologia primaria del paziente, e anche porre l’attenzione su eventuali segni clinico-radiologici precoci compatibili con stadi inziali di MRONJ (prevenzione secondaria) (Tabella 3) (26, 45).
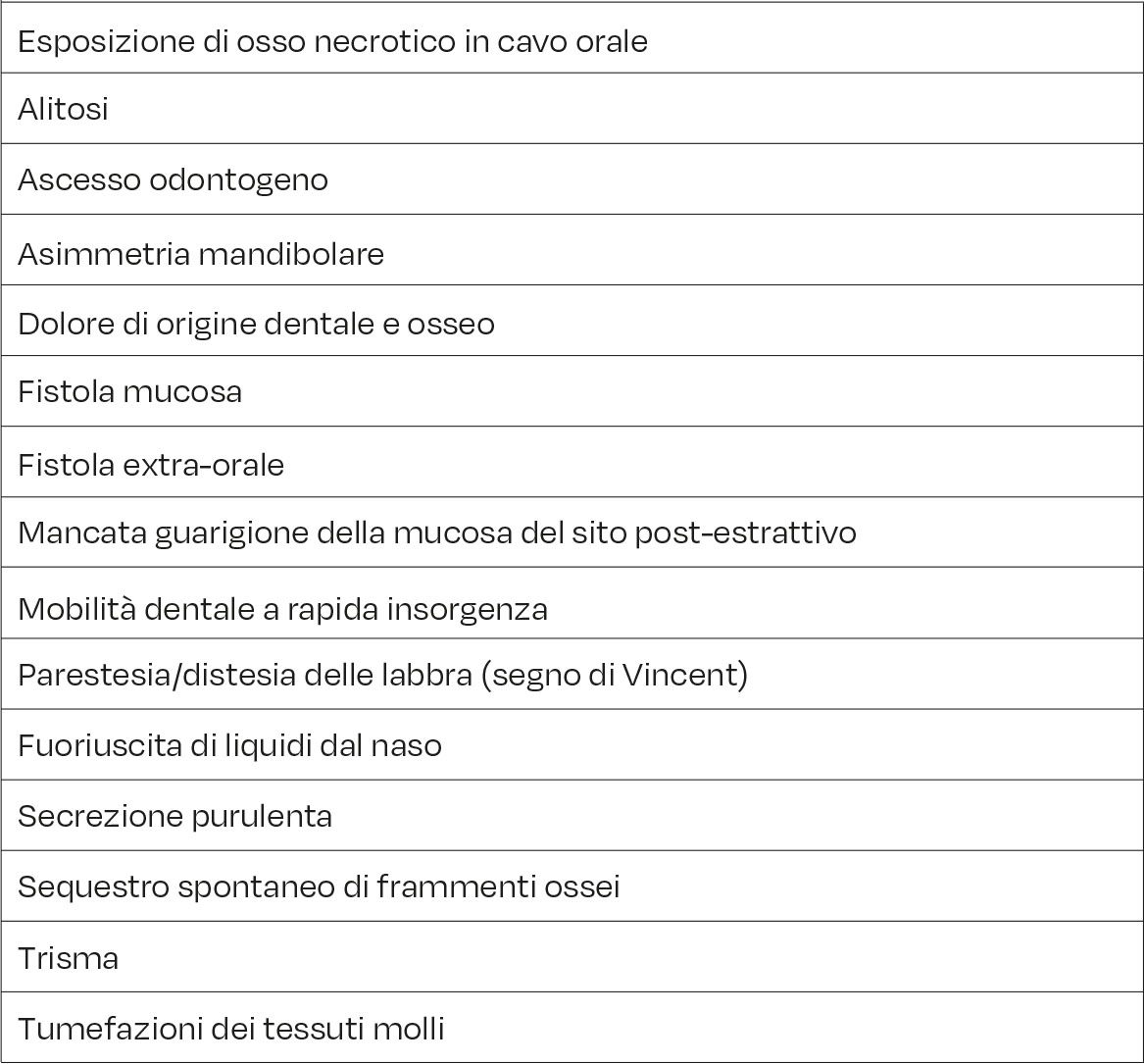

Il board ritiene importante avviare protocolli di prevenzione primaria nei pazienti a rischio di MRONJ. Il percorso di prevenzione orale deve essere sempre avviato, la sua tipologia sarà scelta sulla base dei dati raccolti (e.g., anamnestici, clinici dento-parodontali e radiologici) durante la prima visita odontostomatologica e delle specificità del paziente (e.g., patologia di base, farmaci assunti, comorbidità).
Prevenzione secondaria: ruolo dell’igienista dentale nella diagnosi di sospetto di MRONJ e il timing di follow-up
L’obiettivo principale delle misure di prevenzione secondaria è la diagnosi precoce della malattia.
I pazienti sono definiti affetti da MRONJ se soddisfano i seguenti requisiti (3):
- terapia in atto o pregressa con BMA e/o AA;
- diagnosi clinica e radiologica di progressiva distruzione e necrosi ossea;
- assenza di pregressa o coesistente radioterapia del distretto testa-collo o di neoplasia ossea primitiva e/o metastasi a carico delle ossa mascellari.
Il work-up diagnostico consente al clinico di porre una diagnosi di sospetto (Step 1) e, attraverso la diagnosi differenziale (Step 2), ridurre i tempi per la diagnosi definitiva (Step 3) (Figura 4) (2).
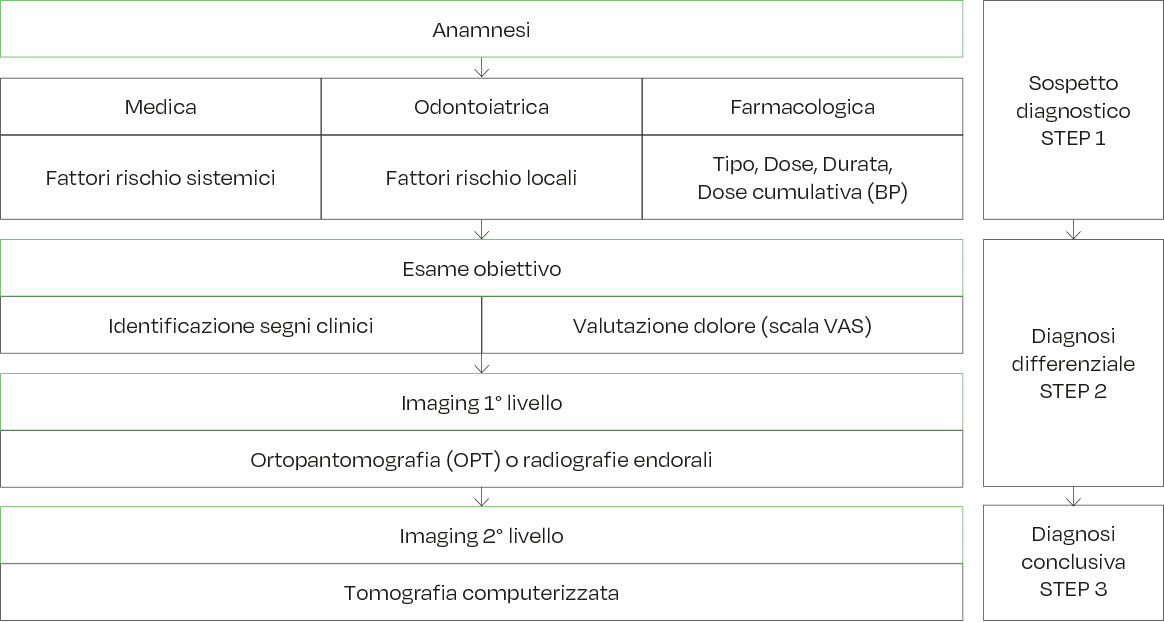
Step 1
L’igienista dentale e l’odontoiatra sono le figure più importanti per la diagnosi precoce di MRONJ in quanto si occupano, entrambi, di prevenzione primaria e di individuare i fattori di rischio locali della patologia (12). Il sospetto di MRONJ dovrebbe essere posto ogni qualvolta un paziente in trattamento (in atto o pregresso) con farmaci definiti a rischio, presenti dei segni e dei sintomi in sede orale, compatibili con MRONJ. La presenza di tali segni clinici deve indurre l’operatore a richiedere accertamenti radiologici per confermare o escludere il sospetto di malattia (46).
Step 2
La diagnosi differenziale deve considerare tutte quelle condizioni patologiche del cavo orale che presentino segni clinici e/o radiologici e/o sintomi sovrapponibili alle fasi iniziali di MRONJ (11). In questa fase l’igienista dentale svolge un importante ruolo attivo anche nel sospetto di diagnosi differenziale tra malattia parodontale, ascessi endo-perio e fasi iniziali di MRONJ, e nell’inviare il paziente, per ulteriori valutazioni, all’odontoiatra o ai centri specializzati per la diagnosi di MRONJ.
Step 3
Il paziente va affidato a centri specializzati per la cura di MRONJ (e.g., Odontoiatra specialista in Chirurgia Orale, ambulatori di Medicina e Patologia Orale, di Chirurgia Orale, di Chirurgia Maxillo-Facciale), che prevede l’esecuzione di indagini radiologiche e strumentali più specifiche, la stadiazione e terapia della malattia (2).
Ruolo dell’Igienista dentale nella terapia di MRONJ
Il ruolo dell’igienista dentale è centrale anche nella terapia della MRONJ, a prescindere se l’approccio scelto sarà di tipo medico o chirurgico, in quanto il mantenimento di un’igiene orale ottimale è il prerequisito minimo per il successo terapeutico della MRONJ.
Una visita collegiale comprensiva di adeguata anamnesi medica e odontoiatrica, valutazione clinico-radiologica mediante esami di I e II livello, definizione dello stadio della MRONJ, valutazione del dolore mediante scala VAS, record fotografico completo è necessaria per l’inquadramento della malattia (2).
A ciò andrà aggiunta una valutazione completa dello stato di salute parodontale (e.g., PSR, CAL, PPD), da registrare in cartella parodontale (21).
La preparazione iniziale e un controllo adeguato professionale della placca batterica orale è in grado di:
- ridurre, quando è presente, la sintomatologia dolorosa accusata da questi pazienti impedendo che i sintomi possano inficiarne la qualità di vita;
- controllare le sovra infezioni minimizzando la progressione della patologia.
Sulla base della salute parodontale/perimplantare del paziente e del quadro clinico generale, si eseguiranno misure di igiene orale professionale minimamente invasive, atte a ristabilire l’igiene orale ottimale e il suo mantenimento. Inoltre, si potranno indicare collutori a base di clorexidina (a diverse concentrazioni in base all’esigenza del momento). Nel caso si decida di trattare la MRONJ con procedure conservative, l’igienista dentale, d’accordo con l’odontoiatra, potrà avere un ruolo centrale in tutte le procedure di biostimolazione tissutale, che possono essere eseguite mediante l’uso di strumenti che generano ozono o mediante laser-terapia (Tabella 5) (47–50).
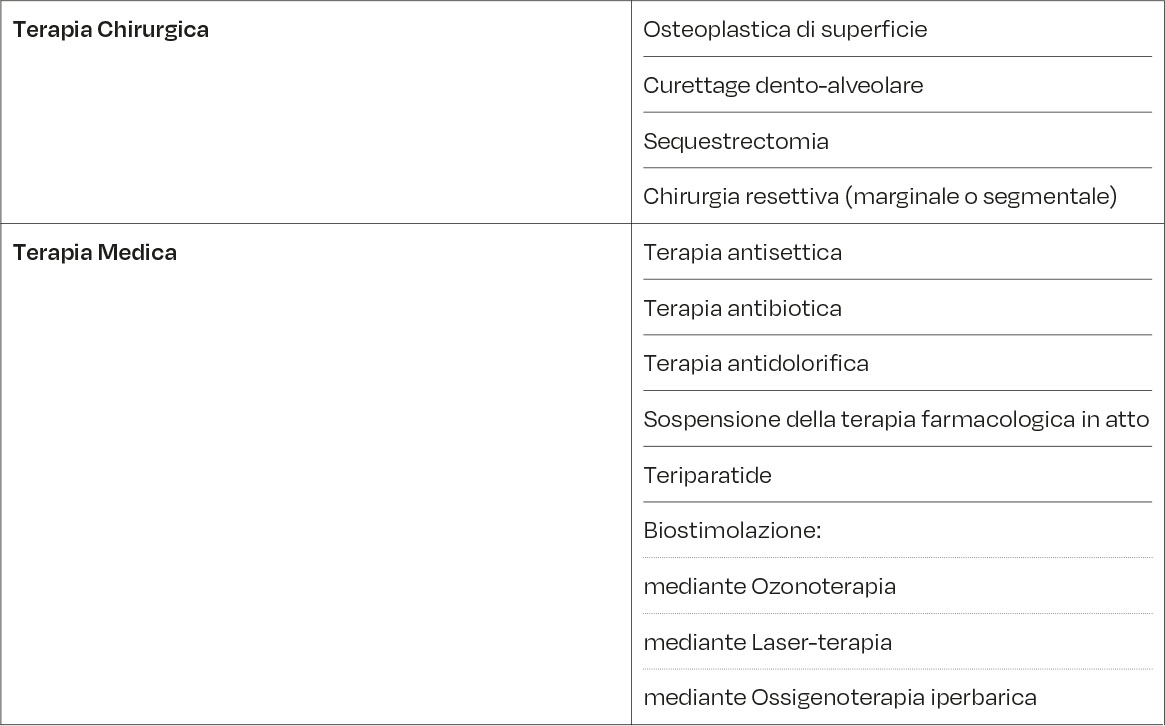
L’ozono agisce con stimolazione e/o conservazione del sistema antiossidante endogeno, attivando la circolazione sanguigna, stimolando reazioni biologiche, esercitando un’azione battericida e riducendo il dolore. Inoltre, è stato riportato che l’ozono favorisca anche il processo di auto-sequestro (51).
L’applicazione dell’Ozonoterapia si avvale di diversi presidi e metodi. Insufflazioni ripetute sembrano stimolare la neoangiogenesi con formazione di tessuto di granulazione, che delimitano aree di osso necrotico con successiva espulsione del sequestro, formazione di tessuto epiteliale e copertura dell’osso sottostante senza ulteriori interventi chirurgici (47–50).
La laserterapia si basa su effetti fotochimici e fotobiologici a carico delle cellule e quindi dei tessuti. Le cellule, stimolate a livello mitocondriale, producono una maggiore quantità di energia, per cui, soprattutto in presenza di deficit funzionali per cause infiammatorie traumatiche o degenerative, tendono ad auto-ripristinare i normali processi fisiologici. Il laser inoltre agisce innalzando la soglia di percezione del dolore tramite azione diretta sulle terminazioni nervose, e indiretta, stimolando la produzione di endorfine; la Low Level Laser Therapy (LLLT), oltre a essere una tecnica sicura e scarsamente invasiva, è ben tollerata (50, 52–55). Molti autori hanno riportato un successo clinico nel trattamento della MRONJ mediante LLLT praticata con diverse lunghezze d’onda e differenti parametri: laser Nd:YAG (1064 nm), a diodi (GaAs – 904 nm), (GaAs – 650, 904-910 nm) (56, 57).
Relativamente alla biostimolazione mediante laser terapia (e.g., LLLT), sembrerebbe essersi dimostrata valida per aumentare la matrice ossea organica in prossimità degli elementi vicini alla lesione e per stimolare la crescita dei vasi sanguigni e linfatici all’interno e all’esterno del solco gengivale, riducendo il dolore ed eventualmente anche le dimensioni dell’esposizione ossea attigua (56, 57).
Per tutti i pazienti candidati alla terapia chirurgica di MRONJ, sarà necessaria una valutazione preliminare dello stato parodontale. Come prima di qualsiasi procedura chirurgica odontoiatrica, se necessario, andranno eseguite sedute di igiene orale professionale personalizzate ed estremamente mininvasive, preferibilmente 7-14 giorni prima, al fine di ridurre la carica batterica e favorire il successo della terapia. Durante tali incontri, saranno indicate al paziente strumenti e tecniche per il controllo della placca domiciliare adeguate e personalizzate per ciascun paziente (21).
Il paziente successivamente verrà sottoposto a visite di controllo periodiche post-chirurgiche per poi rientrare nello schema delle regolari visite di follow-up per la prevenzione primaria della MRONJ (Figura 3).
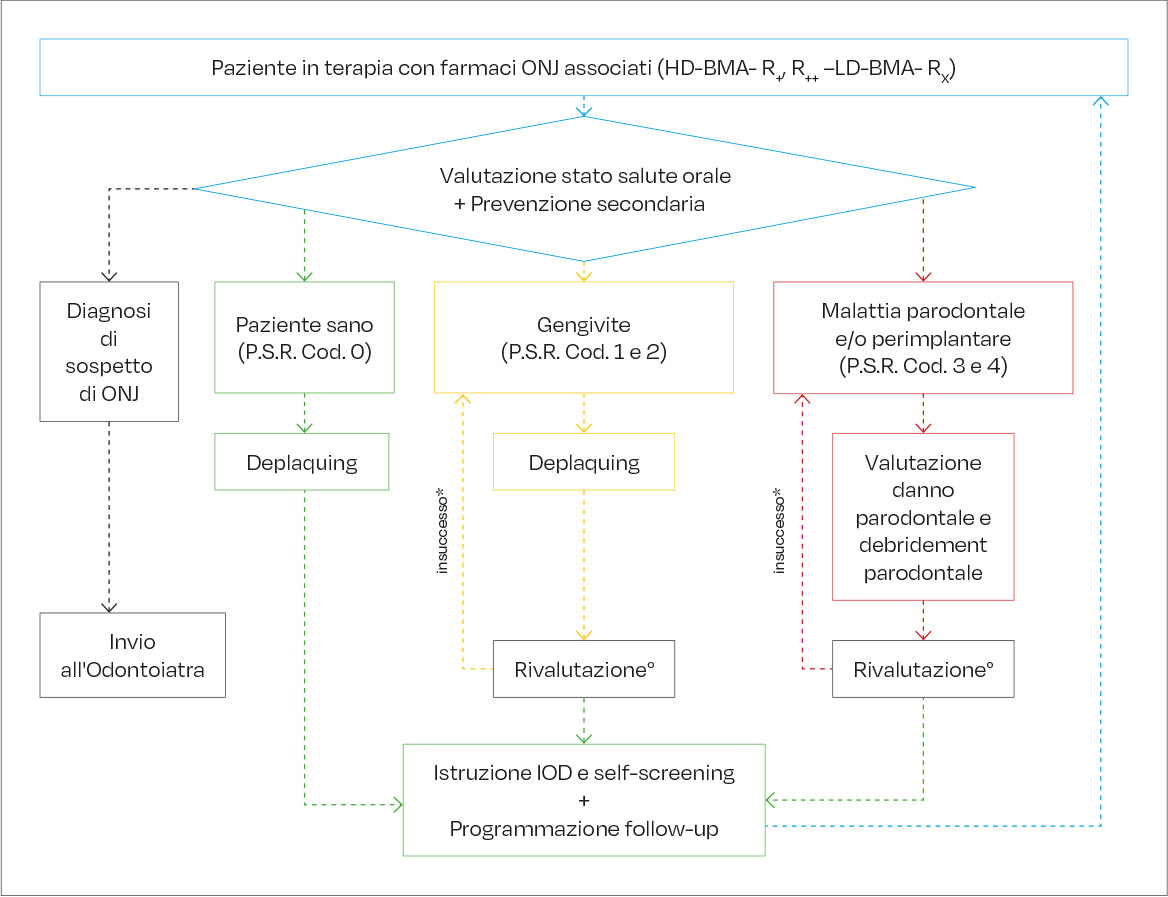
Il Board ritiene che le ultime evidenze scientifiche indichino la necessità di intraprendere tempestivamente la terapia chirurgica di MRONJ. Il ruolo dell’igienista dentale è centrale nella preparazione all’intervento chirurgico, nel mantenimento della salute orale del paziente, nell’applicazione di eventuali terapie adiuvanti la guarigione, e nel follow-up del paziente con pregressa MRONJ o a rischio di svilupparla.
CONCLUSIONI
Alla luce di quanto affermato dalla letteratura scientifica, la prevenzione rappresenta la strategia più efficace nella gestione dei pazienti a rischio di MRONJ, e il ruolo dell’igienista dentale è cruciale in questo contesto. Grazie alla sua formazione specifica e alla frequenza delle visite di controllo, l’igienista dentale svolge un ruolo centrale nell’individuare e monitorare i fattori di rischio locali, contribuendo in modo attivo al ripristino e al mantenimento della salute orale in questa categoria di pazienti. Il riconoscimento dell’importanza del ruolo dell’igienista dentale nell’approccio multidisciplinare è essenziale per garantire una gestione efficace e tempestiva della patologia, riducendone l’incidenza e le complicanze della MRONJ.
1. Bedogni A, Campisi G, Fusco V. Medication Related Osteonecrosis of the Jaw (MRONJ). Qeios; 2018. doi:10.32388/594095
2. Campisi G, Bedogni A, Fusco V. Raccomandazioni Clinico-Terapeutiche Sull’osteonecrosi Delle Ossa Mascellari (ONJ) Farmaco-Relata e Sua Prevenzione. (Srl NDF, ed.). Palermo University Press; 2020. doi:10.19229 /9788855091480/01062020
3. Bedogni A, Mauceri R, Fusco V, et al. Italian position paper (SIPMO-SICMF) on medication-related osteonecrosis of the jaw (MRONJ). Oral Dis. 2024;30(6):3679-3709. doi:10.1111/ODI.14887
4. Campisi G, Fedele S, Fusco V, Pizzo G, Di Fede O, Bedogni A. Epidemiology, clinical manifestations, risk reduction and treatment strategies of jaw osteonecrosis in cancer patients exposed to antiresorptive agents. Future Oncol. 2014;10(2):257-275. doi:10.2217/fon.13.211
5. Fusco V, Santini D, Armento G, Tonini G, Campisi G. Osteonecrosis of jaw beyond antiresorptive (bone-targeted) agents: new horizons in oncology. Expert Opin Drug Saf. 2016;15(7):925-935. doi:10.1080/14740338.2016.1177021
6. Ruggiero SL, Dodson TB, Fantasia J, et al. American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw--2014 update. J Oral Maxillofac Surg. 2014;72(10):1938-1956. doi:10.1016/j.joms.2014.04.031
7. Bagan J, Peydró A, Calvo J, Leopoldo M, Jiménez Y, Bagan L. Medication-related osteonecrosis of the jaw associated with bisphosphonates and denosumab in osteoporosis. Oral Dis. 2016;22(4):324-329. doi:10.1111/odi.12447
8. Troeltzsch M, Woodlock T, Kriegelstein S, Steiner T, Messlinger K, Troeltzsch M. Physiology and pharmacology of nonbisphosphonate drugs implicated in osteonecrosis of the jaw. J Can Dent Assoc. 2012;78(1):c85.
9. Hamadeh IS, Ngwa BA, Gong Y. Drug induced osteonecrosis of the jaw. Cancer Treat Rev. 2015;41(5):455-464. doi:10.1016/j.ctrv.2015.04.007
10. Mauceri R, Coppini M, Attanasio M, et al. MRONJ in breast cancer patients under bone modifying agents for cancer treatment-induced bone loss (CTIBL): a multi-hospital-based case series. BMC Oral Health. 2023;23(1). doi:10.1186/S12903-023-02732-6
11. Mauceri R, Coppini M, Pérez-Sayáns M, et al. Challenges in the diagnosis of oral squamous cell carcinoma mimicking medication-related osteonecrosis of the jaws: a multi-hospital-based case series. Oral Oncol. 2024;151. doi:10.1016/J.ORALONCOLOGY.2024.106689
12. Mauceri R, Arduini S, Coppini M, Bazzano M, Trujillo I, Campisi G. Drug assumption and awareness about adverse drug reactions. The right to know. The case of the bone-modyfing agents: a systematic review. Frontiers in oral health. 2024;5. doi:10.3389/FROH.2024.1441601
13. Vandone AM, Donadio M, Mozzati M, et al. Impact of dental care in the prevention of bisphosphonate-associated osteonecrosis of the jaw: a single-center clinical experience. Ann Oncol. 2012;23(1):193-200. doi:10.1093/annonc/mdr039
14. Owosho AA, Liang STY, Sax AZ, et al. Medication-related osteonecrosis of the jaw: An update on the memorial sloan kettering cancer center experience and the role of premedication dental evaluation in prevention. Oral Surg Oral Med Oral Pathol Oral Radiol. 2018;125(5):440-445. doi:10.1016/j.oooo.2018.02.003
15. Bonacina R, Mariani U, Villa F, Villa A. Preventive strategies and clinical implications for bisphosphonate-related osteonecrosis of the jaw: a review of 282 patients. J Can Dent Assoc. 2011;77:b147.
16. Mah YJ, Kang GY, Kim SJ. Survey on awareness and perceptions of bisphosphonate-related osteonecrosis of the jaw in dental hygienists in Seoul. Int J Dent Hyg. 2015;13(3):222-227. doi:10.1111/idh.12122
17. The role of dental hygienist in the prevention of osteonecrosis of the jaw in patients wearing dentures. doi:10.1586/ERA.1509.1574
18. Rayman S, Almas K, Dincer E. Bisphosphonate-related jaw necrosis: a team approach management and prevention. Int J Dent Hyg. 2009;7(2):90-95. doi:10.1111/j.1601-5037.2008.00331.x
19. Barbato L. BML, CAM, DN, LL, MPCM, OG, RM, RE, RC, SNM, TU, TLP, VE. Terapia anti-riassorbitiva nel paziente osteometabolico affetto da parodontite. Joint position paper della Società Italiana di Ortopedia e Traumatologia (SIOT) e della Società Italiana di Parodontologia e Implantologia (SIdP). Giornale Italiano di Ortopedia e Traumatologia. Published online 2023:1-16. doi:10.32050/0390-0134-xxx
20. Campisi G, Mauceri R, Bertoldo F, et al. Medication-Related Osteonecrosis of Jaws (MRONJ) Prevention and Diagnosis: Italian Consensus Update 2020. Int J Environ Res Public Health. 2020;17(16):1-15. doi:10.3390/IJERPH17165998
21. Mauceri R, Coniglio R, Abbinante A, et al. The preventive care of medication-related osteonecrosis of the jaw (MRONJ): a position paper by Italian experts for dental hygienists. Supportive Care in Cancer. 2022;30(8):6429-6440. doi:10.1007/s00520-022-06940-8
22. Ripamonti CI, Maniezzo M, Campa T, et al. Decreased occurrence of osteonecrosis of the jaw after implementation of dental preventive measures in solid tumour patients with bone metastases treated with bisphosphonates. The experience of the National Cancer Institute of Milan. Annals of Oncology. 2009;20(1):137-145. doi:10.1093/annonc/mdn526
23. Vandone AM, Donadio M, Mozzati M, et al. Impact of dental care in the prevention of bisphosphonate-associated osteonecrosis of the jaw: A single-center clinical experience. Annals of Oncology. 2012;23(1):193-200. doi:10.1093/annonc/mdr039
24. Dimopoulos MA, Kastritis E, Bamia C, et al. Reduction of osteonecrosis of the jaw (ONJ) after implementation of preventive measures in patients with multiple myeloma treated with zoledronic acid. Ann Oncol. 2009;20(1):117-120. doi:10.1093/ANNONC/MDN554
25. Schiodt M, Otto S, Fedele S, et al. Workshop of European task force on medication-related osteonecrosis of the jaw—Current challenges. Oral Dis. 2019;25(7):1815-1821. doi:10.1111/odi.13160
26. Nicolatou-Galitis O, Papadopoulou E, Vardas E, et al. Alveolar bone histological necrosis observed prior to extractions in patients, who received bone-targeting agents. Oral Dis. 2020;26(5):955-966. doi:10.1111/ODI.13294
27. Ministero Del Lavoro, Della Salute e Delle Politiche Sociali Dipartimento Della Qualità Direzione Generale Della Programmazione Sanitaria, Dei Livelli Di Assistenza E Dei Principi Etici Di Sistema Ufficio Iii Raccomandazione Per La Prevenzione Dell’osteonecrosi Della Mascella/Mandibola Da Bifosfonati.; 2009.
28. Ministero Della Salute Dipartimento Della Sanità Pubblica e Dell’innovazione Raccomandazioni per La Promozione Della Salute Orale, La Prevenzione Delle Patologie Orali e La Terapia Odontostomatologica Nei Pazienti Adulti Con Malattia Neoplastica.; 2014.
29. James P, Worthington H V., Parnell C, et al. Chlorhexidine mouthrinse as an adjunctive treatment for gingival health. Cochrane Database of Systematic Reviews. 2017;2017(3). doi:10.1002/14651858.CD008676.pub2
30. Esther M. Wilkins. La Pratica Clinica Dell’Igienista Orale.; 2017.
31. Cairo F, Carrassi A, Paoli S De, Roccuzzo M, Trombelli L. La diagnosi in parodontologia. Published online 2020:1-16.
32. Felton D, Cooper L, Duqum I, et al. Evidence-Based Guidelines for the Care and Maintenance of Complete Dentures: A Publication of the American College of Prosthodontists. Journal of Prosthodontics. 2011;20(SUPPL. 1):S1-S12. doi:10.1111/j.1532-849X.2010.00683.x
33. Schiodt M, Otto S, Fedele S, et al. Workshop of European task force on medication-related osteonecrosis of the jaw-Current challenges. Oral Dis. 2019;25(7):1815-1821. doi:10.1111/ODI.13160
34. Di Fede O, Panzarella V, Mauceri R, et al. The dental management of patients at risk of medication-related osteonecrosis of the jaw: New paradigm of primary prevention. Biomed Res Int. 2018;2018. doi:10.1155/2018/2684924
35. Sanz M, Herrera D, Kebschull M, et al. Treatment of stage I–III periodontitis—The EFP S3 level clinical practice guideline. J Clin Periodontol. 2020;47(S22):4-60. doi:10.1111/jcpe.13290
36. James P, Worthington H V., Parnell C, et al. Chlorhexidine mouthrinse as an adjunctive treatment for gingival health. Cochrane Database of Systematic Reviews. 2017;2017(3). doi:10.1002/14651858.CD008676.pub2
37. Brookes ZLS, Bescos R, Belfield LA, Ali K, Roberts A. Current uses of chlorhexidine for management of oral disease: a narrative review. J Dent. 2020;103:103497. doi:10.1016/j.jdent.2020.103497
38. Cobb CM, Daubert DM, Davis K, et al. Consensus Conference Findings on Supragingival and Subgingival Air Polishing. Compend Contin Educ Dent. 2017;38(2):e1-e4.
39. Ulvik IM, Sæthre T, Bunæs DF, Lie SA, Enersen M, Leknes KN. A 12-month randomized controlled trial evaluating erythritol air-polishing versus curette/ultrasonic debridement of mandibular furcations in supportive periodontal therapy. BMC Oral Health. 2021;21(1). doi:10.1186/s12903-021-01397-3
40. Wilson WR, Gewitz M, Lockhart PB, et al. Prevention of Viridans Group Streptococcal Infective Endocarditis: A Scientific Statement from the American Heart Association. Circulation. 2021;143(20):E963-E978. doi:10.1161/CIR.0000000000000969
41. Caton JG, Armitage G, Berglundh T, et al. A new classification scheme for periodontal and peri-implant diseases and conditions – Introduction and key changes from the 1999 classification. J Periodontol. 2018;89(S1):S1-S8. doi:10.1002/JPER.18-0157
42. Papapanou PN, Sanz M, Buduneli N, et al. Periodontitis: Consensus report of workgroup 2 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. Published online June 1, 2018.
43. Chapple ILC, Mealey BL, Van Dyke TE, et al. Periodontal health and gingival diseases and conditions on an intact and a reduced periodontium: Consensus report of workgroup 1 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89:S74-S84. doi:10.1002/JPER.17-0719
44. Berglundh T, Armitage G, Araujo MG, et al. Peri-implant diseases and conditions: Consensus report of workgroup 4 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89:S313-S318. doi:10.1002/JPER.17-0739
45. Rasmusson L, Abtahi J. Bisphosphonate associated osteonecrosis of the jaw: An update on pathophysiology, risk factors, and treatment. Int J Dent. 2014;2014. doi:10.1155/2014/471035
46. Lo Russo L, Lo Muzio L, Buccelli C, Di Lorenzo P. Bisphosphonates-related osteonecrosis of the jaws: Medicolegal issues. Oral Dis. 2013;19(4):425-426. doi:10.1111/odi.12049
47. Goker F, Donati G, Grecchi F, et al. Treatment of BRONJ with ozone/oxygen therapy and debridement with piezoelectric surgery. Eur Rev Med Pharmacol Sci. 2020;24(17):9094-9103. doi:10.26355/eurrev_202009_22855
48. Suh Y, Patel S, Kaitlyn R, et al. Clinical utility of ozone therapy in dental and oral medicine. Med Gas Res. 2019;9(3):163-167. doi:10.4103/2045-9912.266997
49. Ripamonti CI, Maniezzo M, Boldini S, Pessi MA, Mariani L, Cislaghi E. Efficacy and tolerability of medical ozone gas insufflations in patients with osteonecrosis of the jaw treated with bisphosphonates-Preliminary data Medical ozone gas insufflation in treating ONJ lesions. J Bone Oncol. 2012;1(3):81-87. doi:10.1016/j.jbo.2012.08.001
50. Souza Tolentino E, Castro TF, Michellon FC, et al. Adjuvant therapies in the management of medication-related osteonecrosis of the jaws: Systematic review. Head Neck. 2019;41(12):4209-4228. doi:10.1002/hed.25944
51. Suh Y, Patel S, Kaitlyn R, et al. Clinical utility of ozone therapy in dental and oral medicine. Med Gas Res. 2019;9(3):163-167. doi:10.4103/2045-9912.266997
52. Vescovi P, Manfredi M, Merigo E, et al. Early surgical laser-assisted management of bisphosphonate-related osteonecrosis of the jaws (BRONJ): a retrospective analysis of 101 treated sites with long-term follow-up. Photomed Laser Surg. 2012;30(1):5-13. doi:10.1089/pho.2010.2955
53. Chambrone L, Wang HL, Romanos GE. Antimicrobial photodynamic therapy for the treatment of periodontitis and peri-implantitis: An American Academy of Periodontology best evidence review. J Periodontol. 2018;89(7):783-803. doi:10.1902/jop.2017.170172
54. Lin Z, Strauss FJ, Lang NP, Sculean A, Salvi GE, Stähli A. Efficacy of laser monotherapy or non-surgical mechanical instrumentation in the management of untreated periodontitis patients. A systematic review and meta-analysis. Clin Oral Investig. 2021;25(2):375-391. doi:10.1007/s00784-020-03584-y
55. Minamisako MC, Ribeiro GH, Lisboa ML, Mariela Rodríguez Cordeiro M, Grando LJ. Medication-Related Osteonecrosis of Jaws: A Low-Level Laser Therapy and Antimicrobial Photodynamic Therapy Case Approach. Case Rep Dent. 2016;2016:1-4. doi:10.1155/2016/6267406
56. Vescovi P, Merigo E, Meleti M, et al. Conservative surgical management of stage i bisphosphonate-related osteonecrosis of the jaw. Int J Dent. 2014;2014:107690. doi:10.1155/2014/107690
57. Romeo U, Galanakis A, Marias C, et al. Observation of pain control in patients with bisphosphonate-induced osteonecrosis using low level laser therapy: preliminary results. Photomed Laser Surg. 2011;29(7):447-452. doi:10.1089/pho.2010.2835






